¿Conoces la importancia de determinar y analizar los riesgos del sistema? ¿En qué etapa del ciclo de la vida del sistema debemos realizar esta evaluación?
Conoce la respuesta a estas intrigantes preguntas en este blog, recuerda que si tienes alguna duda puedes dejarla abajo en los comentarios y la responderemos de inmediato o puedes mandárnosla a nuestro correo: hola@qbd.lat
¿Por qué es importante determinar los riesgos del sistema antes de la validación?
Principalmente para determinar el alcance de la validación e implementar controles que disminuyan los riesgos detectados a un nivel aceptable o los eliminen.
Se requiere el conocimiento a detalle de los riesgos propios del sistema de acuerdo a su categoría, antigüedad, complejidad y grado de personalización, así como del proceso al cual sirve el sistema.
Entre mayor información se tenga al respecto, mejor controlados podrán estar los riesgos, ya que tendremos datos sobre los controles implementados.
La Guía GAMP® 5 recomienda que el riesgo se elimine a través de modificaciones en los procesos o el diseño del sistema. Las revisiones del diseño pueden jugar un papel clave en la eliminación del riesgo desde un inicio.
Los riesgos que no pueden ser eliminados desde el diseño deben ser reducidos a un nivel aceptable a través de la implementación de controles.
La reducción de riesgos incluye la aplicación de controles para disminuir la severidad y la ocurrencia e incrementar la detectabilidad.
Se debe tener un enfoque sistemático para verificar que el riesgo asociado a un sistema ha sido eliminado o reducido a un nivel aceptable.
El alcance de la verificación y el nivel de detalle de la documentación deberán estar basadas en el riesgo hacia la salud del paciente, calidad del producto, la integridad de datos principalmente, sin dejar de tomar en cuenta la complejidad del sistema.
Es importante mencionar que el análisis de riesgos…
Forma parte del sistema de Gestión de Riesgos implementado en cada empresa y debe ser gestionado conforme a lo establecido por cada organización.
Existen varias herramientas para llevar a cabo los análisis de riesgos, entre otras: HACCP, HAZOP; AMEF.
La herramienta AMEF es reconocida por la WHO como las más adecuadas para el entorno farmacéutico.
De manera general, se considera que a mayor criticidad y complejidad del sistema, aumenta su riesgo inherente.
La evaluación del riesgo se hará dependiendo de la etapa del ciclo de vida en la que se encuentre el sistema.
Más adelante se abordará el análisis de riesgos hacia los Requisitos de Usuario y durante el mantenimiento del estado validado.
Análisis de Riesgo al sistema Una vez que se han identificado los riesgos de acuerdo a la categoría del sistema, se debe determinar el impacto de dichos riesgos en los siguientes rubros:
1) Salud del paciente
2) calidad del producto
3) Integridad de datos
4) cumplimiento normativo
5) Cumplimiento a las políticas internas de la organización
6) Impacto al negocio
Si se emplea un enfoque integral de evaluación de los riesgos en función del cumplimiento normativo, cumplimiento a políticas internas, cuidando la integridad de los datos y el impacto al negocio, se contribuirá a preservar la calidad del producto y por lo tanto la salud del paciente.
Estos dos últimos puntos, se considera medular en la evaluación del impacto BPx de los riesgos ya identificados para cada sistema y debe quedar documentado, al igual que la categorización del sistema (Ver Tema Categorías de los sistemas computarizados) para justificar las subsiguientes etapas de la validación.
La determinación del impacto deberá estar apoyada en las herramientas del sistema de gestión de riesgos implementado por la organización.
Las organizaciones pueden tener un proceso de gestión del riesgo establecido, incluyendo el uso de métodos que describe la Guía GAMP® 5, sin embargo, también podrán emplearse los métodos que se describen en la guía ICHQ9.
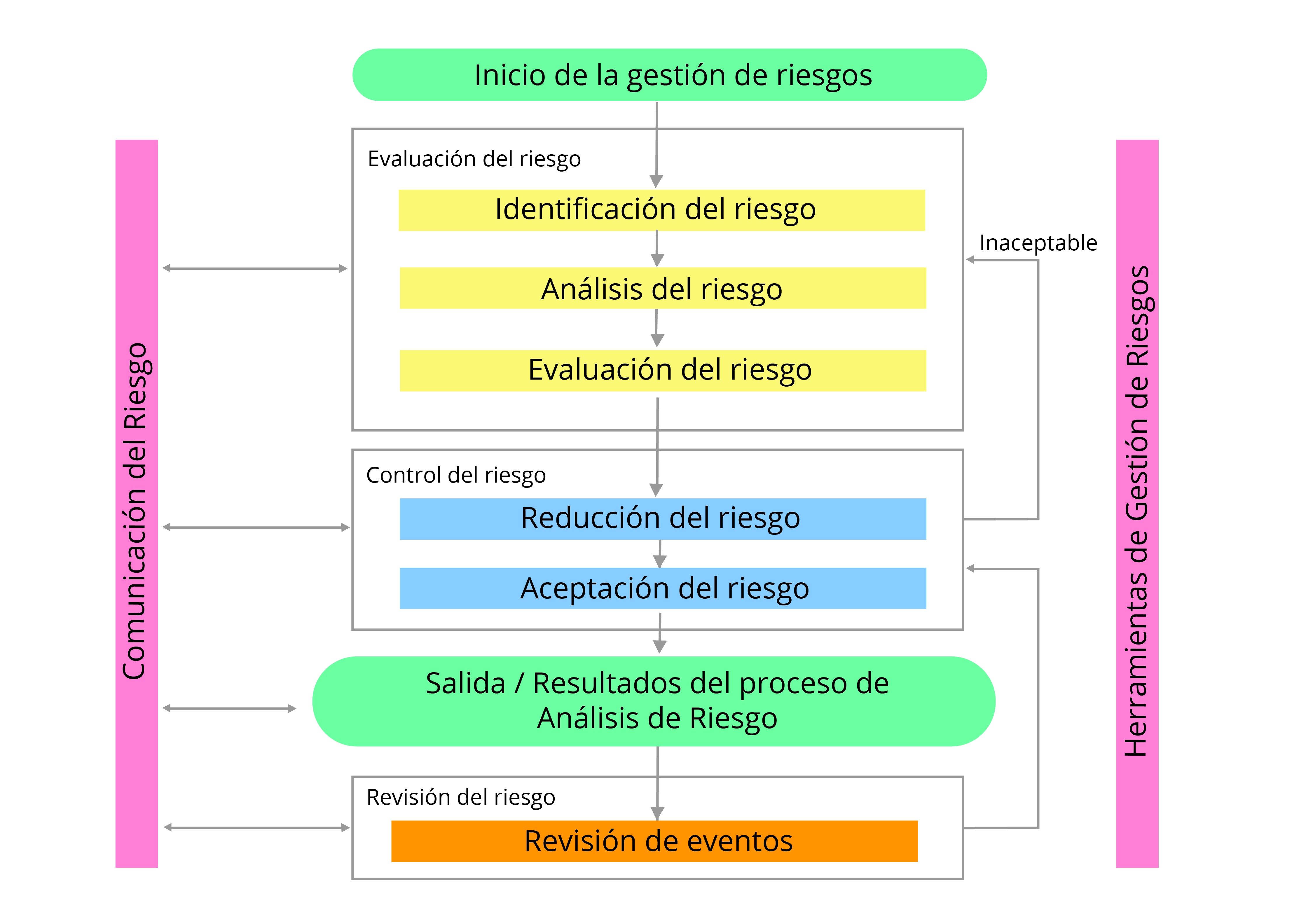
La metodología elegida será la que resulte más funcional, de acuerdo al proceso. El siguiente diagrama esquematiza y resume las etapas de un sistema de gestión de riesgos:
¡RECUERDA! EN WWW.QBD.LAT TE PODEMOS AYUDAR CON:
Validación de Sistemas Computarizados Validación de Procesos | Validación de Limpieza | Validación de hojas de cálculo | Cualificación de Equipos | Cualificación de Sistemas de Apoyo Crítico (HVAC) | Evaluación clínica, regulatoria y Validación de Medical Devices | Data Integrity |
Contáctanos en: hola@qbd.lat
- Norteamérica: (+55) 5516 6646
- Suramérica: (+57) 350-8886031
- Europa: (+34) 655 591 603
¡Únete a nuestra comunidad en redes!



